サイケデリック物質DMTが、たった一度の投与でうつ病モデルマウスの認知機能と快楽消失を改善するという画期的な研究成果が明らかになりました。本記事では、ブラジルの研究チームが発表した最新の動物実験の結果をもとに、DMTがどのように脳の神経新生を促進し、うつ病症状を改善するのかを詳しく解説します。
DMT単回投与で実証されたうつ病症状の改善効果

この研究の最も重要な発見は、DMTの単回投与が慢性ストレスで誘発されたうつ病様症状を劇的に改善したという点です。実験では、慢性予測不可能軽度ストレス(UCMS)モデルと呼ばれる、うつ病の中核症状である快楽消失を再現できる動物モデルが使用されました。
研究チームは、56日間のストレス曝露後にDMT(30mg/kg)を単回投与したマウスと、従来の抗うつ薬フルオキセチンを30日間連日投与したマウスの反応を比較しました。その結果、DMT投与群では快楽消失の指標である糖水嗜好性が著しく改善し、行動絶望のテストでも無動時間が大幅に減少したのです。さらに、パターン分離能力として知られる認知機能テストにおいても、DMT投与マウスは対照群と比較して明確な改善を示しました。
特筆すべきは、DMTの効果が慢性フルオキセチン治療をほとんどの指標で上回ったという点です。フルオキセチン群では糖水嗜好性の回復が部分的であったのに対し、DMT投与群ではストレスを受けていないマウスと同等レベルまで回復しました。この結果は、DMTが従来の抗うつ薬よりも迅速かつ強力な治療効果を持つ可能性を示唆しています。
海馬神経新生の促進メカニズムと異所性細胞の減少
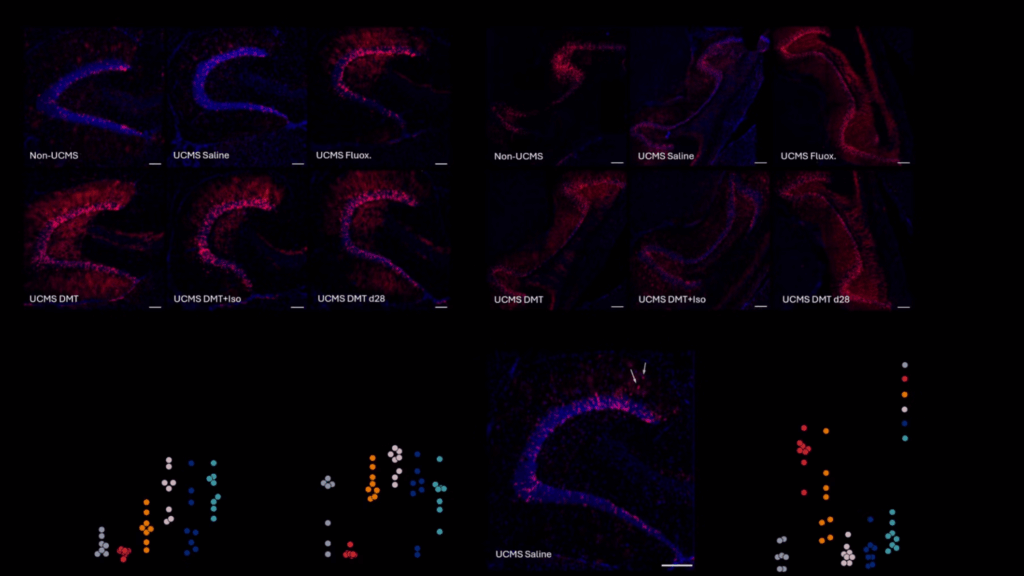
DMTの抗うつ作用の背後には、成体海馬神経新生の顕著な増加という神経生物学的変化がありました。海馬は記憶や感情調節に関わる脳領域であり、その歯状回という部位では成体になっても新しい神経細胞が生まれ続けています。この神経新生のプロセスは、うつ病の発症と回復において重要な役割を果たすと考えられています。
組織学的分析の結果、DMT投与マウスでは海馬の背側部と腹側部の両方で新生神経細胞の数が著しく増加していました。特に背側海馬では、ストレスを受けていない対照群をも上回る神経新生が確認されました。これは単なるストレス効果の逆転ではなく、神経新生の純増を意味します。フルオキセチン群と比較すると、DMT群は腹側海馬で約2倍の新生細胞数を示し、慢性薬物治療よりも強力な神経新生促進効果を持つことが明らかになりました。
さらに重要な発見として、DMT投与は異所性顆粒細胞の数を劇的に減少させました。異所性細胞とは、本来あるべき顆粒細胞層から20μm以上離れた場所に誤って組み込まれた新生神経細胞のことです。慢性ストレスを受けたマウスではこの異所性細胞が増加し、海馬回路の正常な機能を妨げると考えられています。DMT投与群では異所性細胞数がストレスを受けていない対照群と同等レベルまで減少し、正常な神経回路の統合が回復したことが示されました。
相関分析では、異所性細胞の数と行動症状との間に強い負の相関関係が認められました。異所性細胞が多いマウスほど糖水嗜好性が低く(r = -0.67)、認知課題の成績も悪い(r = -0.42)という結果が得られました。これは、異所性神経新生の抑制がDMTの治療効果の重要なメカニズムである可能性を強く示唆しています。
セロトニン受容体と神経栄養因子の役割
DMTは主に5-HT2A受容体を介して作用しますが、5-HT1Aや5-HT2C受容体にも結合します。これらの受容体はすべて神経新生の異なる段階に関与しています。5-HT2A受容体は前駆細胞の増殖と神経分化を促進し、5-HT1A受容体は神経前駆細胞の増殖と生存を調節し、5-HT2C受容体は後期前駆細胞の生存と分化に影響を与えます。
また、DMTは脳由来神経栄養因子(BDNF)やシグマ1受容体の活性化を通じて、神経可塑性を促進することも知られています。これらの分子経路は、新生神経細胞の成熟と海馬回路への機能的統合において重要な役割を果たすと考えられます。DMTの効果が複数の受容体システムを通じて媒介されることが、その広範で強力な治療効果の基盤となっている可能性があります。
ストレス期間中のDMT投与と予防的効果の検証

研究チームは、ストレス曝露の途中である28日目にDMT を投与するという独自の実験群も設定しました。この実験デザインの目的は、ストレスが進行中であってもDMTが保護的効果を示すかを検証することでした。
結果は部分的な成功を示しました。ストレス期間中にDMT投与を受けたマウス(DMT-d28群)は、快楽消失の発症が著しく抑制され、糖水嗜好性がストレスを受けていない対照群と同等レベルに維持。また、行動絶望テストでも無動時間の短縮が認められ、抗うつ様効果が確認されました。神経新生についても、腹側海馬では対照群の約2倍の増加が見られ、異所性細胞の数も減少していました。
しかし、認知機能に関しては改善が見られなかったとのこと。パターン分離課題において、DMT-d28群のマウスはストレス後にDMTを投与された群と異なり、有意な成績向上を示しませんでした。この結果は、DMTの効果が領域特異的である可能性を示唆しています。つまり、快楽や動機づけに関わる情動的側面は早期介入で保護できるものの、認知機能の回復にはストレス終了後の投与がより効果的である可能性があります。
この差異の理由として、タモキシフェン投与のタイミングが考えられるとされています。すべてのマウスはストレス期間の終盤にタモキシフェンを投与され、新生神経細胞が蛍光タンパク質で標識されました。そのため、DMT-d28群で観察された神経新生は、DMT投与の直接的効果というよりも、ストレス後の回復期における持続的な影響を反映している可能性があります。にもかかわらず、この群が快楽消失に対して保護効果を示したことは、DMTの単回投与が長期的な神経保護効果を持つことを示唆しています。
イソフルラン麻酔下での効果と意識体験の必要性

サイケデリック療法において最も議論されている問題の一つが、主観的なサイケデリック体験が治療効果に必要かどうかという点です。この問いに初期的な知見を提供するため、研究チームはイソフルラン麻酔下でDMTを投与する実験群を設定しました。
麻酔下でDMTを投与されたマウス(DMT+Iso群)は、覚醒状態でDMTを投与されたマウスと同様の行動改善を示しました。糖水嗜好性は有意に回復し、行動絶望テストでも無動時間が減少し、認知課題の成績も向上しました。さらに、神経新生の増加と異所性細胞の減少も確認されました。これらの結果は、DMTの治療効果が意識的なサイケデリック体験なしでも発現する可能性を示唆しています。
ただし、この解釈には重要な注意点があります。イソフルランそのものが抗うつ作用を持つことが報告されており、TrkB シグナル伝達を活性化することが知られています。一方で、イソフルランは海馬前駆細胞の増殖を抑制し、認知機能を低下させるという報告もあります。本研究では神経新生の増加と認知機能の改善が観察されたため、これらの効果がイソフルラン単独では説明できないことを示唆していますが、イソフルラン単独投与群が設定されていないため、確定的な結論は導けません。
興味深いことに、最近の研究では、5-HT2A受容体の活性化を薬理学的に阻害してもサイケデリックの治療効果が維持されることが示されています。これは、サイケデリックが意識体験とは独立した神経栄養因子のシグナル伝達経路を通じて作用する可能性を支持します。将来的には、抗うつ特性を持たないハロタンなどの麻酔薬を用い、麻酔単独群を含めた実験デザインにより、この問題をより明確にする必要があります。
まとめ:DMTは神経回路修復を通じた迅速な抗うつ薬となる可能性
この研究は、DMTの単回投与が慢性ストレス誘発性うつ病モデルにおいて快楽消失、行動絶望、認知障害を劇的に改善することを実証しました。これらの行動改善は、海馬における成体神経新生の著しい増加と、異所性顆粒細胞の正常化という神経生物学的変化と密接に関連していました。DMTの効果は従来の抗うつ薬フルオキセチンを上回り、さらに麻酔下でも効果が維持される可能性が示されました。
これらの知見は、DMTが神経回路レベルの修復を標的とした迅速作用型抗うつ薬として開発される可能性を強く支持します。特に、従来のセロトニン再取り込み阻害薬に反応しない治療抵抗性うつ病患者にとって、新たな治療選択肢となることが期待されます。ただし、本研究はオスのマウスのみを対象としており、性差の影響や用量反応関係、効果の持続期間など、臨床応用に向けて解明すべき課題も残されています。
今後は、DMTの作用機序をさらに詳細に解明し、幻覚作用を持たない非サイケデリック性類似体の開発や、最適な投与プロトコルの確立が求められます。神経新生の促進と回路統合の正常化というDMTの独自のメカニズムは、うつ病治療のパラダイムシフトをもたらす可能性を秘めています。
Lima da Cruz, R. V., Costa, R. B. G. de M., de Queiroz, G. M., Stojanovic, T., Moulin, T. C., & Leão, R. N. (2026). Single-dose DMT reverses anhedonia and cognitive deficits via restoration of neurogenesis in a stress-induced depression model. Translational Psychiatry. https://doi.org/10.1038/s41398-026-03852-7
本記事は情報提供のみを目的としており、医療アドバイスではありません。
精神的・身体的な問題を抱えている方は、必ず医療専門家にご相談ください。
また、日本国内でのサイケデリック物質の所持・使用は法律で禁止されています。



