従来の抗うつ薬では改善が困難とされる治療抵抗性うつ病において、サイケデリック療法が画期的な治療成果を示しています。2025年7月に発表されたBPL-003の臨床試験結果は、単回投与で8週間にわたる持続的な抗うつ効果を実証し、メンタルヘルス治療の新時代を告げるものです。
BPL-003の臨床試験で治療抵抗性うつ病に劇的改善効果を確認
2025年7月1日、atai Life SciencesとBeckley Psytechが共同で発表した治療抵抗性うつ病(TRD)患者を対象としたBPL-003のフェーズ2b臨床試験結果は、サイケデリック療法の可能性を大きく広げるものでした。
この二重盲検プラセボ対照試験では、193名の患者が参加し、8mgまたは12mgのBPL-003を単回投与された群において、プラセボ群と比較して統計学的に有意な抗うつ効果が確認されました。特に注目すべきは、投与から24時間後という早期の段階で効果が現れ、8週間後まで持続したことです。
主要評価項目であるMADRS(Montgomery-Åsberg Depression Rating Scale)スコアの変化では、8mg投与群で平均12.1ポイント、12mg投与群で平均11.1ポイントの改善が見られ、これは臨床的に意味のある大幅な改善を示しています。
atai Life Sciences:サイケデリック医療のパイオニア企業

BPL-003を開発するatai Life Sciences(NASDAQ: ATAI)は、精神的健康治療の変革を目指すドイツ生まれの、臨床段階のバイオ医薬品会社です。2018年に設立された同社は、Compass PathwayやMindMedなどとともに、サイケデリックベースの治療法開発における世界的リーダーとして位置づけられています。
同社の特徴的なアプローチは、複数のサイケデリック化合物を同時並行で開発している点にあるでしょう。BPL-003以外にも、DMT(ジメチルトリプタミン)を用いたVLS-01、R-MDMAを基盤とするEMP-01、統合失調症に伴う認知機能障害を対象とするRL-007など、多様な精神疾患に対する治療選択肢を開発中です。
atai Life Sciencesの主要パイプライン
- BPL-003(メブフォテニン):治療抵抗性うつ病 – フェーズ3準備完了
- VLS-01(DMT):治療抵抗性うつ病 – フェーズ2進行中
- EMP-01(R-MDMA):社会不安障害 – フェーズ2a進行中
- RL-007:統合失調症に伴う認知機能障害 – フェーズ2b進行中
2025年には、Beckley Psytechとの戦略的合併により、サイケデリック治療分野における包括的なリーダーシップの確立を目指しています。この合併により、BPL-003の開発がさらに加速されると期待されています。
治療抵抗性うつ病とは何か?従来治療の限界

治療抵抗性うつ病とは、現在のうつ病エピソードにおいて2つ以上の抗うつ薬治療に反応しない状態を指します。うつ病患者の約50%がこの条件に該当すると推定されており、世界規模で約3億人のうつ病患者のうち、約1億5000万人が治療抵抗性うつ病に苦しんでいる計算になります。
従来の治療法では、SSRI(選択的セロトニン再取り込み阻害薬)やSNRI(セロトニン・ノルアドレナリン再取り込み阻害薬)などの抗うつ薬が主流でしたが、これらの薬物は効果発現まで数週間から数か月を要し、また約3分の1の患者では十分な効果が得られないという課題がありました。
現在、治療抵抗性うつ病に対して承認されている治療選択肢は限られており、エスケタミン鼻腔スプレー(Spravato®)や電気けいれん療法(ECT)などがありますが、これらも完全な解決策とは言えない状況でした。
そんな中、近年はLSDやシロシビンといったサイケデリックを用いたサイケデリック療法の研究が世界中で進められています。また、アメリカではオレゴン州やコロラド州が合法化を進めるなど、各国で制度の確立が始まっています。
BPL-003(メブフォテニン)の特徴と作用機序
atai Life Sciencesが開発中の製剤「BPL-003」は、5-MeO-DMT(ブフォテニン)のベンゾエート塩を有効成分とする鼻腔内投与製剤です。5-MeO-DMTは、セロトニン5-HT1A/5-HT2A受容体に作用する化合物で、「クラシックサイケデリック」と呼ばれる、従来のサイケデリック化合物とは異なる薬理学的プロファイルを示すとされています。
この化合物の最大の特徴は、なんと言っても、作用時間の短さです。投与後約2時間で効果が減弱するため、患者は短時間のクリニック滞在で治療を完了することができます。これは、6-8時間の滞在が必要なシロシビンや、さらに長時間を要するLSDなどの他のサイケデリック化合物と比較して、大幅な患者負担軽減を意味するのです。
また、BPL-003は既に承認されている鼻腔スプレーデバイスを使用して投与されるため、静脈内注射などの侵襲的な方法を必要としません。この投与方法により、現在のSpravato®治療で確立された2時間のクリニック治療パラダイムに適合できる可能性があるとされ、期待が高まっています。
フェーズ2b臨床試験の詳細結果
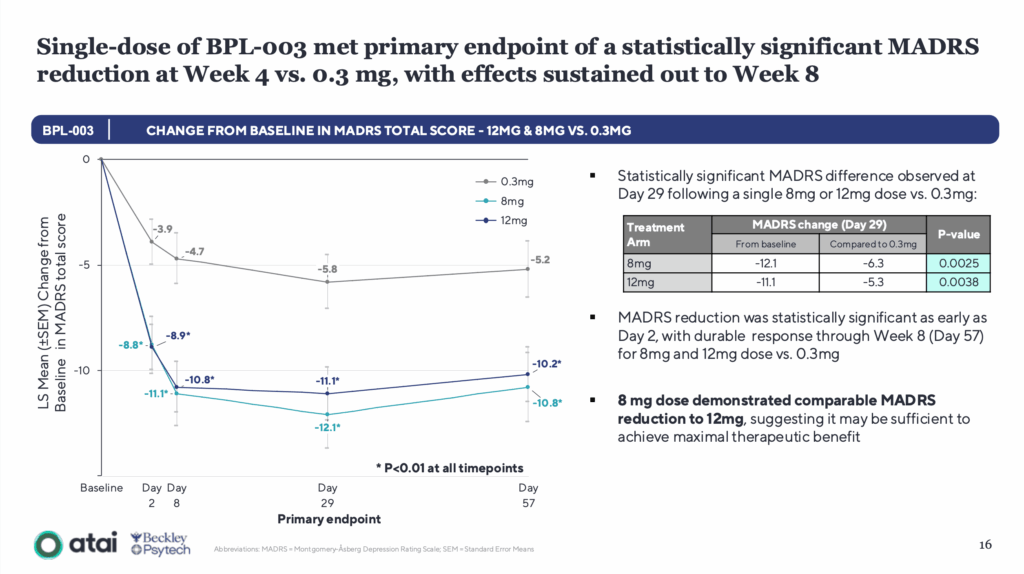
今回の臨床試験は、6か国38施設で実施された史上最大規模のメブフォテニン対照試験であり、米国を含む盲検フェーズ2試験としては初めてのものでした。試験デザインは、0.3mg、8mg、12mgの3群に患者を無作為に割り付ける四重盲検試験として設計されました。
有効性の結果
- 8mg群:MADRS スコア改善 -12.1ポイント(対照群比 -6.3ポイント、p=0.0025)
- 12mg群:MADRS スコア改善 -11.1ポイント(対照群比 -5.3ポイント、p=0.0038)
- 効果は投与2日目から確認され、8週間持続
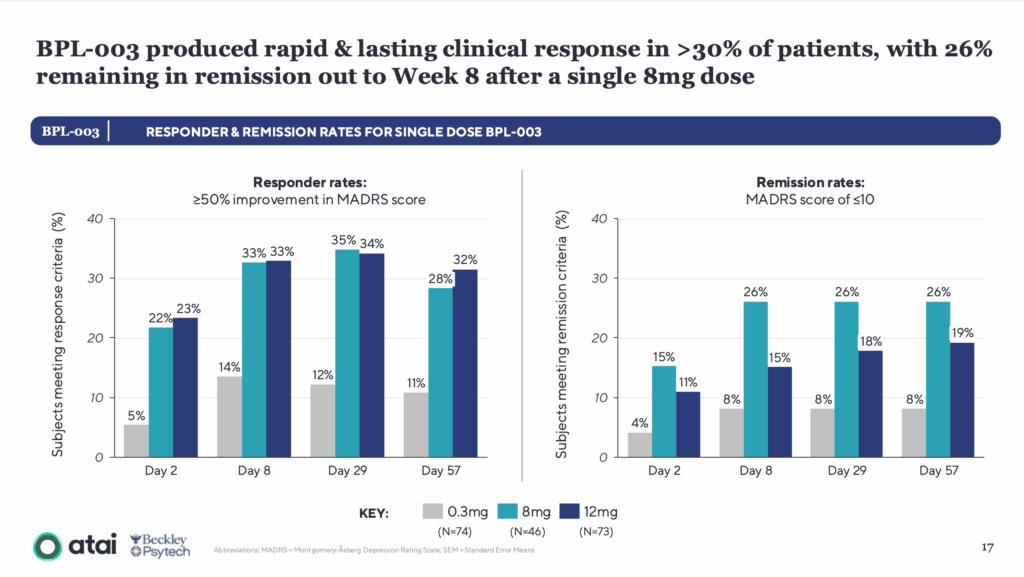
反応率と寛解率
- 8mg群:投与29日目の反応率33%、寛解率26%
- 12mg群:投与29日目の反応率34%、寛解率18%
- 効果は投与57日目(8週間後)まで維持
これらの結果は、単回投与で長期間にわたる抗うつ効果が得られることを示しており、従来の毎日服薬が必要な抗うつ薬とは根本的に異なる治療アプローチの可能性を示唆しています。
短時間治療による患者負担軽減の可能性
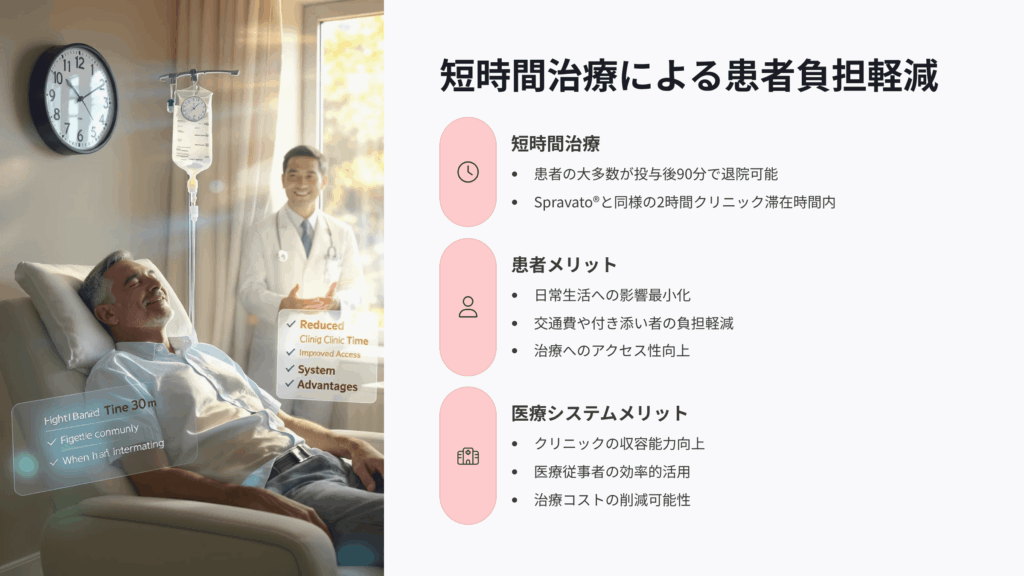
BPL-003治療の革新的な側面の一つは、その治療時間の短さです。臨床試験では、患者の大多数が投与後90分の時点で退院可能な状態と判定されました。これは、現在のSpravato®治療で確立された2時間のクリニック滞在時間内に収まる結果です。
この短時間治療が実現する利点は多岐にわたります。患者にとっては、仕事や日常生活への影響最小化、交通費や付き添い者の負担軽減、治療へのアクセス性向上といったメリットがあります。医療システムにとっては、クリニックの収容能力向上、医療従事者の効率的活用、治療コストの削減可能性が期待されます。保険制度にとっても、従来治療と比較した費用対効果の改善や、長期入院や集中治療の回避という利点があります。
これらの利点により、BPL-003は既存の医療インフラに容易に統合できる可能性があり、サイケデリック療法の普及における大きな障壁を取り除く可能性があります。
サイケデリック療法の安全性と副作用
BPL-003の安全性プロファイルは良好であることが確認されました。臨床試験において、治療関連重篤有害事象(SAE)は報告されず、治療中止に至った有害事象も稀であったとのこと。
10%以上の患者で報告された主な副作用として、投与部位の痛み・不快感が25%、悪心が21%、頭痛が19%、血圧上昇が11%の患者で確認されました。これらの副作用の99%以上は軽度から中等度であり、多くは投与当日に解消されました。血圧や心拍数の一時的上昇は見られましたが、平均的には投与後1時間以内にベースライン値に戻りました。
他にも重要な点としては、自殺関連安全性シグナルは観察されなかったことにあります。8mgおよび12mg投与群において、治療後の自殺念慮や自殺行動の発現は報告されておらず、これは治療抵抗性うつ病治療における重要な安全性指標です。
今後の展望とサイケデリック医療の未来

BPL-003の成功は、サイケデリック療法の商業化への道筋を大きく前進させるものと言えるでしょう。atai Life SciencesとBeckley Psytechは、この結果を受けてFDAとの協議を予定しており、フェーズ3試験への移行を目指しています。
短期的な展望として、今後1-2年でフェーズ3試験の開始、規制当局との協議進展、製造体制の確立が期待されています。さらに、中期的には3-5年をかけて規制承認の取得、医療従事者への研修体制構築、治療ガイドライン策定が進むと予想されます。長期的には5-10年の期間で標準治療としての確立、他の精神疾患への適応拡大、次世代サイケデリック治療薬の開発が見込まれています。
また、BPL-003の成功は、他のサイケデリック化合物の開発にも好影響を与えると予想されます。シロシビン、MDMA、LSDなど、様々な化合物による治療法の研究が加速し、精神医療分野における選択肢の多様化につながるかもしれません。
まとめ:サイケデリック療法が開く新たな治療の扉
BPL-003のフェーズ2b臨床試験結果は、サイケデリック療法が単なる実験的治療から実用的な医療選択肢へと転換する重要な転換点を示しています。単回投与による長期持続効果、短時間治療、良好な安全性プロファイルという3つの特徴は、従来の精神医療の枠組みを根本的に変革する可能性を秘めています。
治療抵抗性うつ病に苦しむ数百万人の患者にとって、BPL-003は希望の光となるかもしれません。また、この成功は他のサイケデリック化合物の研究開発を促進し、うつ病以外の精神疾患治療における新たな可能性も広げるでしょう。
今後数年間で、我々はサイケデリック療法の実用化という歴史的瞬間を目撃することになるかもしれません。科学的根拠に基づいた慎重なアプローチのもとで、これらの革新的治療法が一人でも多くの患者の人生を改善することを期待したいと思います。
atai Life Sciences and Beckley Psytech Announce Positive Topline Results from the Phase 2b Study of BPL-003 in Patients with Treatment-Resistant Depression | Atai Life Sciences N.V. (n.d.). Atai Life Sciences N.V. https://ir.atai.life/news-releases/news-release-details/atai-life-sciences-and-beckley-psytech-announce-positive-topline
本記事は情報提供のみを目的としており、医療アドバイスではありません。
精神的・身体的な問題を抱えている方は、必ず医療専門家にご相談ください。
また、日本国内でのサイケデリック物質の所持・使用は法律で禁止されています。



