サイケデリック医療の世界で画期的な進展が報告されました。治療抵抗性うつ病患者を対象としたBPL-003の第2b相臨床試験延長研究で、2回目の投与により追加的な抗うつ効果が確認され、患者の約半数が寛解に至ったことが明らかになりました。本記事では、この革新的な鼻腔スプレー型サイケデリック治療薬の最新データと、今後の展望について紹介します。
動画の解説はこちら
BPL-003の反復投与により治療抵抗性うつ病の寛解率が大幅に向上

バイオ医薬品企業AtaiBeckley社が2025年11月10日に発表した臨床試験結果により、BPL-003(メブフォテニン安息香酸鼻腔スプレー)の2回目投与が治療抵抗性うつ病患者に対して有意な追加効果をもたらすことが実証されました。初回投与から8週間後に12mgの2回目投与を行った結果、アクティブドーズ群では63%の患者が反応基準を満たし、48%が寛解基準を達成しました。この結果は、従来の抗うつ薬では改善が見られなかった患者にとって、新たな希望となる可能性を示しています。
BPL-003とは:短時間作用型の鼻腔スプレー製剤
BPL-003は、メブフォテニン安息香酸という物質を鼻腔スプレーで投与する革新的な治療薬候補です。
メブフォテニン安息香酸の正体
メブフォテニンは、化学的には5-ヒドロキシ-DMT(5-HO-DMT)とも呼ばれる天然のトリプタミン系化合物です。実は自然界では、ヒキガエルの皮膚腺から分泌される防御物質として知られています。構造的には、アヤワスカに含まれるDMT(ジメチルトリプタミン)の近縁物質で、脳内のセロトニン受容体、特に5-HT2A受容体に作用することで抗うつ効果をもたらすと考えられています。
「安息香酸塩」という形態にすることで、この物質を医薬品として安定化させ、鼻腔から効率的に吸収できるようにしています。鼻腔投与は、飲み薬のように消化器官を通過する必要がないため、より速やかに血中に到達し、効果発現までの時間が短縮されます。また、注射による投与と比べて患者の負担が少ないという利点もあります。
短時間作用型という革新性
BPL-003の最大の特徴は、サイケデリック体験の持続時間が短いことにあります。従来のシロシビン療法では数時間にわたる体験セッションが必要でしたが、BPL-003では平均して投与後2時間以内に退院基準を満たすことができると言います。
この短時間作用型という特性は、医療現場への統合という観点で非常に重要です。長時間のセッションを必要とする治療法は、医療施設の負担が大きく、患者にとってもスケジュール調整が困難です。BPL-003は既存の精神科医療インフラに組み込みやすい設計となっており、実用化された際の普及可能性が高いと期待されています。
さらに注目すべきは、米国食品医薬品局(FDA)からブレークスルー治療指定を受けている点です。これは、重篤な疾患に対する画期的な治療法として、優先的な審査を受けられる制度です。この指定を受けることで、開発プロセスが加速され、より早く患者のもとへ届く可能性が高まります。
治療抵抗性うつ病という深刻な問題
治療抵抗性うつ病とは、2種類以上の抗うつ薬による治療を試みても十分な改善が見られないうつ病のことを指します。研究によれば、うつ病患者の最大50%がこの治療抵抗性うつ病に該当する可能性があります。世界中で約3億人がうつ病に苦しんでいることを考えると、1億5000万人もの人々が既存の治療法では十分な効果が得られていない計算になります。
治療抵抗性うつ病は、単に症状が続くだけでなく、不安障害、性機能障害、認知機能障害などの併存症の発症率が高く、生活の質も著しく低下します。患者本人だけでなく、介護者や医療システムにも大きな負担をかけており、新たな治療選択肢の開発は喫緊の課題となっています。
第2b相臨床試験の詳細結果
オープンラベル延長研究の設計
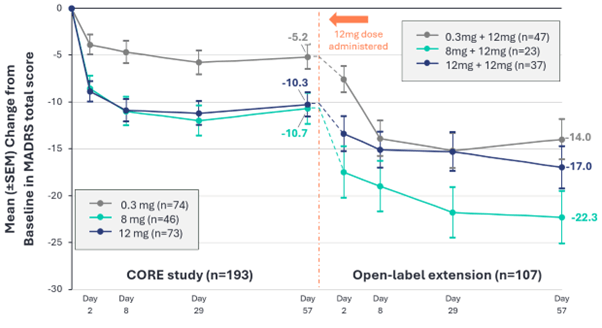
今回発表されたのは、第2b相臨床試験のオープンラベル延長研究(OLE)の結果です。この試験は2つの段階で構成されていました。まず8週間のブラインド試験(コア試験)で、患者は0.3mg、8mg、または12mgのBPL-003を1回投与されました。その後、コア試験を完了した126名のうち107名が延長研究に参加し、初回投与時の用量や抑うつ症状のスコアに関わらず、全員が8週間後に12mgの2回目投与を受けました。
用量別の有効性データ
最も興味深い結果は、初回投与時の用量によって2回目投与後の効果が異なった点です。
コア試験で0.3mg(低用量対照群)を受けた患者47名では、2回目の12mg投与後、モンゴメリー・アスベルグうつ病評価尺度(MADRS)スコアが平均14.0ポイント減少しました。これは、実質的に初回アクティブドーズを受けたのと同様の抗うつ効果が得られたことを意味します。
一方、コア試験で8mgを受けた患者23名では、驚くべき結果が見られました。2回目投与後のMADRSスコアの減少は平均22.3ポイントに達し、81%が反応基準を満たし、67%が寛解基準を達成しました。これは、初回投与で既に効果があった患者が、2回目投与によってさらに症状が改善したことを示しています。
アクティブドーズ(8mgまたは12mg)を受けた全患者60名を統合して分析すると、2回目投与後のMADRSスコアは平均19.0ポイント減少し、63%が反応基準、48%が寛解基準を満たしました。これらの効果は最大8週間持続し、合計で約4か月間の抗うつ効果が得られたことになります。
安全性と忍容性のプロファイル
安全性の面でも、BPL-003は良好な結果を示しました。副作用の大部分は投与当日に発生し、その多くは軽度から中等度で一過性のものでした。最も頻繁に報告された副作用は、吐き気、頭痛、投与部位の痛みや不快感、血圧上昇、不安などでした。
重要な点として、薬剤関連の重篤な有害事象は2回目投与後8日目に1件報告されましたが、入院監視とサポートにより回復しました。それ以外に薬剤関連の重篤な有害事象は報告されませんでした。
この安全性プロファイルは、BPL-003の以前の試験結果や、他のサイケデリック療法で報告されているものと概ね一致しており、全体として良好な忍容性を示しています。投与後平均2時間以内に退院基準を満たせるという点も、既存の精神科治療パラダイムに統合しやすいことを裏付けています。
間欠投与パラダイムの実現可能性

今回の研究が示した最も重要な意義の一つは、間欠投与(一定期間を空けて複数回投与すること)のパラダイムが実現可能であることを実証した点です。8週間の間隔を空けた2回の投与で、合計約4か月間の抗うつ効果が得られたという事実は、患者と医療提供者の両方にとって大きなメリットとなります。
従来の抗うつ薬は毎日服用する必要があり、服薬アドヒアランス(処方通りに薬を飲み続けること)が課題となっていました。また、効果が現れるまでに数週間かかることも珍しくありません。対照的に、BPL-003は単回投与で迅速な効果が得られ、その効果が数週間持続します。これは患者の負担を大幅に軽減し、治療継続率の向上にもつながる可能性があります。
さらに、短時間のサイケデリック体験と組み合わせた間欠投与モデルは、医療施設の運営効率も向上させることが期待されます。1回のセッションが2時間程度で完結するため、1日により多くの患者を治療できる可能性があります。これは、治療を必要とする多くの患者にアクセスを提供する上で極めて重要な要素となります。
FDAとの協議と第3相試験への道筋

AtaiBeckley社は、FDAとの第2相終了後ミーティングを予定しています。このミーティングでは、第3相臨床試験の設計やその他の開発プログラムの詳細について協議が行われます。同社は2026年第1四半期に第3相プログラムに関するガイダンスを提供し、FDAミーティングの結果を踏まえて、2026年第2四半期に第3相臨床試験を開始する予定です。
今回のデータにより、8mg用量を第3相開発に進めることが支持されました。また、反復投与により抗うつ効果が継続・増強される可能性も示されたため、第3相試験では単回投与だけでなく、複数回投与のプロトコルも検討される可能性があります。
サイケデリック医療の新時代
BPL-003の開発は、サイケデリック医療の新たな潮流を象徴しています。従来のシロシビンやMDMA補助療法が長時間のセッションと集中的な心理療法を必要とするのに対し、BPL-003は短時間作用型で、既存の医療インフラに組み込みやすい設計となっています。
日本においても、治療抵抗性うつ病は深刻な問題です。既存の治療法で十分な効果が得られない患者にとって、このような新しい治療選択肢の登場は希望の光となるでしょう。ただし、サイケデリック療法は必ず医療専門家の厳格な監督下で実施される必要があり、自己治療は絶対に避けなければなりません。
BPL-003が承認されれば、短時間で効果が現れ、数週間持続し、間欠的な投与で維持できるという特性により、うつ病治療のパラダイムを大きく変える可能性があります。
まとめ:治療抵抗性うつ病に新たな希望をもたらす可能性
BPL-003の第2b相臨床試験延長研究は、治療抵抗性うつ病に対する革新的なアプローチの実現可能性を示しました。8週間間隔での2回投与により、患者の約半数が寛解に達し、効果は約4か月間持続しました。短時間作用型という特性と良好な安全性プロファイルにより、既存の医療システムへの統合が期待されます。
2026年に予定されている第3相臨床試験の結果次第では、数年以内に新たな治療選択肢として利用可能になる可能性があります。世界中で1億人以上が既存の治療法では十分な効果が得られていない現状を考えると、BPL-003のような革新的な治療法の開発は、精神医療の未来を大きく変える可能性を秘めています。
ただし、これはまだ臨床試験段階の治療法であり、承認されるまでには更なる研究が必要です。サイケデリック療法に興味がある方は、必ず医療専門家に相談し、臨床試験への参加機会について情報を得ることが重要です。
AtaiBeckley Announces Positive Topline Data from the Phase 2b Open-Label Extension Study of BPL-003, Supporting Safety and Efficacy of a Second Dose in Patients with Treatment-Resistant Depression | AtaiBeckley N.V. (n.d.). AtaiBeckley N.V. https://ir.ataibeckley.com/news-releases/news-release-details/ataibeckley-announces-positive-topline-data-phase-2b-open-label
本記事は情報提供のみを目的としており、医療アドバイスではありません。
精神的・身体的な問題を抱えている方は、必ず医療専門家にご相談ください。
また、日本国内でのサイケデリック物質の所持・使用は法律で禁止されています。



