サイケデリック物質が依存症治療において新たな可能性を持つことが科学的研究で明らかになってきています。本記事では、アルコール依存症やタバコ依存症などの治療におけるサイケデリック療法の歴史的背景、最新研究、神経科学的メカニズム、そして将来性について詳しく紹介します。
サイケデリック療法とは何か
サイケデリック療法とは、LSD(リゼルグ酸ジエチルアミド)やシロシビン(マジックマッシュルームに含まれる成分)などの物質を医療管理下で使用し、心理療法と組み合わせる治療法です。これらの物質は脳内のセロトニン2A受容体に作用し、意識状態の一時的な変化をもたらします。

サイケデリック療法には主に3つの段階があります。
- 準備段階(プレパレーション): 患者が精神的に準備を整え、治療の目的や意図を明確にします。
- セッション段階: サイケデリック物質を服用し、専門のガイドとともに体験を深めます。
- 統合段階(インテグレーション): 体験から得た洞察を日常生活に取り入れる段階です。
依存症治療におけるサイケデリック研究の歴史
LSDの初期研究
サイケデリック物質の治療利用は新しいものではありません。1950年代から60年代にかけて、LSDを用いたアルコール依存症治療の研究が盛んに行われていました。
2012年にKrebsとJohansenが行ったメタ分析によると、536名の参加者を対象とした6つのランダム化比較試験において、LSDはプラセボと比較して明確な治療効果を示しました(オッズ比1.96; 95% CI, 1.36–2.84; p=0.0003)。特筆すべきは、この効果サイズが現在のアルコール依存症治療薬(ナルトレキソン:オッズ比0.69)を大きく上回っていることです。LSDグループでは、フォローアップ時に59%の患者が改善を示したのに対し、プラセボグループでは38%でした。また、完全禁酒に関しても、3ヶ月時点でLSD群はプラセボ群と比較して有意に高い成功率を示しました(オッズ比1.80; CI 1.07–3.04)。
1970年代には、ヘロイン依存症患者78名を対象とした研究も行われました。LSD支援療法(300-350μg)を受けたグループは、通常の集団精神療法を受けたグループと比較して、12ヶ月後の時点で33%が禁断を維持していたのに対し、対照群では5%にとどまりました。尿検査で生物学的に確認されたこの結果は、当時としては画期的でした。
しかし、1970年に規制物質法が施行され、LSDやシロシビンなどのサイケデリック物質がスケジュール1(医学的使用価値がなく、乱用の可能性が高いとされる物質)に分類されたことで、これらの研究は長らく停滞していました。サイケデリックに関する否定的な宣伝、効果への疑念、関連研究分野(例:統合失調症)への資金配分などの要因も、サイケデリック研究を次第に減少させました。
2000年代に入り、科学的関心が再び高まり、現在は「サイケデリック・ルネサンス」と呼ばれる研究の活性化が起きています。
最新の臨床研究からわかること
シロシビンとアルコール依存症
近年の研究では、シロシビンがアルコール依存症の治療に有望な結果を示しています。
Bogenschutzらが2015年に行ったパイロット研究では、DSM-IVの基準でアルコール依存症の診断を受けた10名の患者を対象に研究を実施しました。参加者は4週目(21mg/70kg)と8週目(28mg/70kg)にシロシビンセッションを2回受け、さらに動機付け強化療法7セッション、準備セッション3回、事後振り返りセッション2回を含む心理社会的介入を12セッション受けました。
結果として、大量飲酒日の割合はベースラインと比較して5-12週目の間で有意に減少し(平均差26.0%、95% CI = 8.7–43.2、p = 0.008)、この効果は36週間の追跡期間全体を通じて維持されました。飲酒日の割合と大量飲酒日の両方がベースラインと比較して有意に低いままでした。副作用はすべて軽度で、5名の患者が頭痛を報告し、1名が吐き気、下痢、不眠を報告しました。
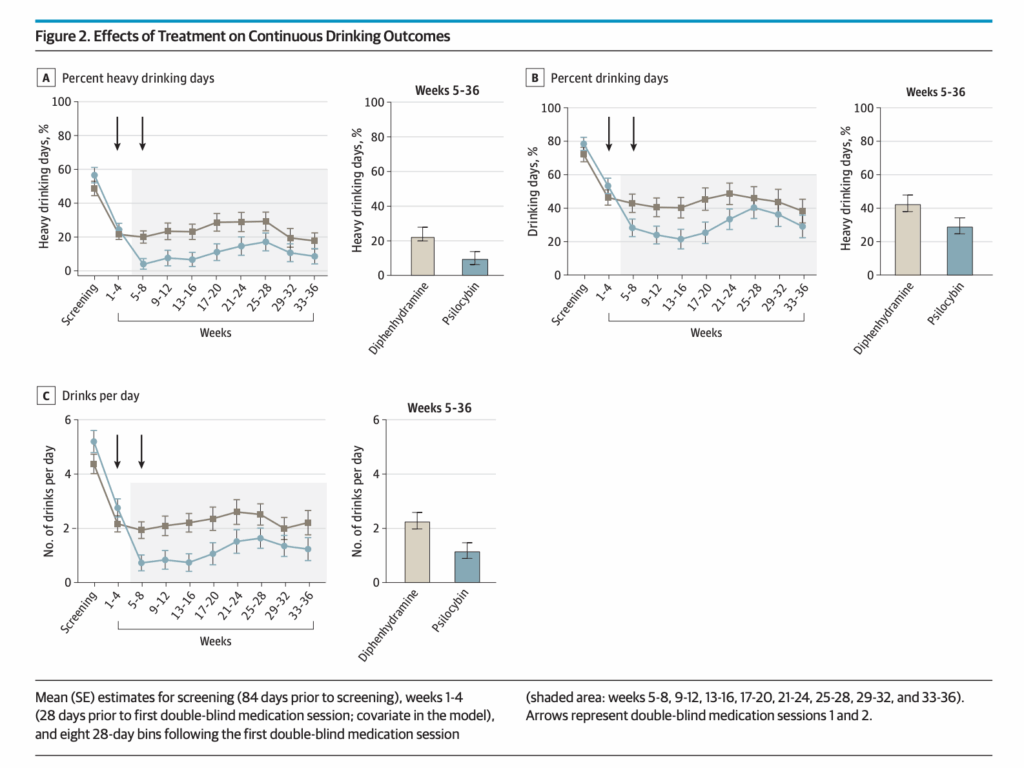
近年のさらなる研究では、Bogenschutzらによる二重盲検プラセボ対照無作為化試験が実施され、95名のアルコール依存症患者が参加しました。参加者はシロシビンまたはプラセボ(ジフェンヒドラミン)のいずれかに1:1で無作為に割り当てられました。シロシビン治療群の患者は4週目(25 mg/70 kg)と8週目(25-40 mg/70 kg)に2回のセッションを受け、心理社会的介入も行われました。32週間の二重盲検期間中、大量飲酒日の割合はシロシビン群で9.7%、ジフェンヒドラミン群で23.6%であり、平均差は13.9%(95% CI = 3.0-24.7、p = 0.01)でした。平均アルコール消費量(1日あたりの標準飲酒単位数)もシロシビン群で有意に低かったことが示されました。
シロシビンとタバコ依存症

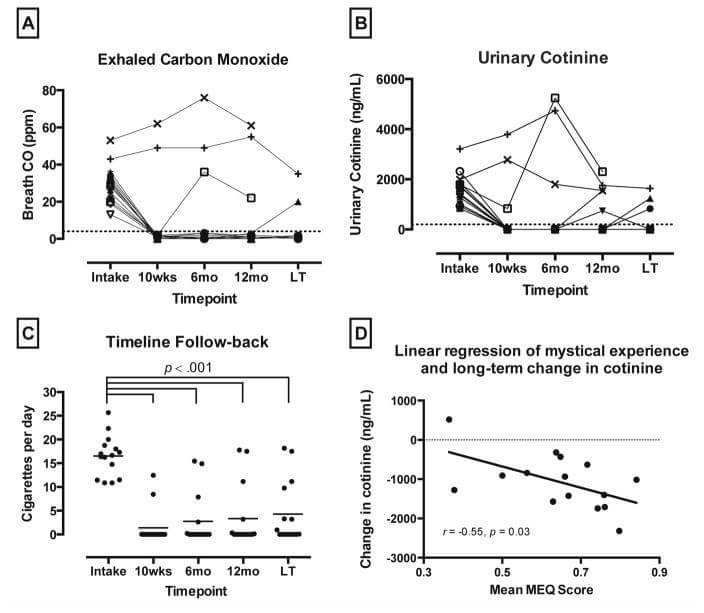
Johnson らがジョンズ・ホプキンス大学で実施した単群オープンラベル研究では、禁煙を求める15名を対象に、禁煙のためのCBTと2-3回のシロシビン投与(初回20mg/70kg、後続30mg/70kg)を組み合わせた15週間の介入を行いました。参加者は平均6回の禁煙試行歴があり、31年間にわたって1日平均19本のタバコを吸っていました。
結果は主観的質問票と呼気一酸化炭素および尿中コチニンレベルによる生化学的検査の両方で定量化されました。15名中12名(80%)が6ヶ月後のフォローアップで生化学的に確認された禁煙状態を示し、これらの個人のうち11/12が最初のシロシビン投与後に禁煙したと報告しました。この予備的研究は、最良の行動療法や薬物療法と比較して、治療後6ヶ月の時点で禁煙率が著しく高いことを示しました(通常は35%未満)。
さらに、長期追跡調査では、52週(1年)後の時点で15名中10名(67%)が禁煙を維持していました。アルコール依存症の研究と同様に、神秘的体験のスコアが高いほど、より良い転帰と相関していました。
他の依存症に関する研究
コカイン使用障害に関しては、アラバマ大学で二重盲検ランダム化試験が実施されており、初期の非公開結果によれば、シロシビンを投与された最初の10人の患者は、プラセボ群と比較して生活満足度が高く、うつ症状が少なく、コカインの断薬日数が多かったことが示されています。
メタンフェタミン依存症については、メタンフェタミン依存症の30名の成人を対象に、25mgと30mgのシロシビンをそれぞれ2回投与する群と通常治療を受ける群を比較する無作為化試験が進行中です。この研究の結果は2024年6月に予定されています。
オピオイド使用障害(OUD)については、ブプレノルフィン-ナロキソン維持療法を受けている患者におけるシロシビンの安全性と相互作用を調査する小規模オープンラベル安全性研究が行われています。このような研究は、薬物間相互作用の可能性を理解し、これらの薬物で維持療法を受けているOUD患者の安全性を確保するために重要です。
治療メカニズムと効果
サイケデリック療法が依存症に効果を発揮するメカニズムはまだ完全には解明されていませんが、いくつかの重要な要素が明らかになっています。
- 神経可塑性の促進: サイケデリック物質は脳の神経接続を新たに形成する「神経可塑性」を高める可能性があります。
- デフォルトモードネットワークの変調: 脳の「デフォルトモードネットワーク」と呼ばれる領域の活動パターンが変化し、過去の習慣や思考パターンから抜け出す助けとなります。
- 神経伝達物質システムの調整: サイケデリックはセロトニン系だけでなく、ドーパミン系にも影響を与え、依存症に関連する報酬系の機能を改善する可能性があります。
- 精神的・心理的変化: 依存症は「意識の狭窄と固定化」と捉えることができますが、サイケデリック体験は意識を拡大し、新たな視点や洞察をもたらすことで、依存行動から抜け出す手助けとなります。
多くの研究で、サイケデリック体験の強度(特に「神秘的体験」の度合い)と治療効果の間に相関関係が見られています。
まとめ:サイケデリック療法は依存症治療の新たな選択となるか
日本における依存症問題と必要性
厚生労働省の統計によれば、日本のアルコール依存症患者は約100万人に達すると推計されていますが、実際に治療を受けているのはわずか4%程度です。また、薬物依存症の再犯率は約65%、ギャンブル等依存症の有病率は成人の約3.6%(320万人)と報告されています。現行の治療法は再発率が高く、アルコール依存症患者の約半数が1年以内に再発するという厳しい現実があります。
日本の依存症治療は認知行動療法や自助グループが中心で、薬物療法の選択肢は限られています。このような状況を考えると、新たな治療法の開発は喫緊の課題です。海外で有望な結果を示しているサイケデリック療法は、既存の治療に反応しない患者や再発を繰り返す患者に対する新たな選択肢となる可能性があります。
今後の展望
現在、世界各国でアルコール、タバコ、コカイン、オピオイド、メタンフェタミンなどの依存症を対象とした臨床試験が進行中です。今後数年で第3相臨床試験の結果が出揃い、医療認可に向けた動きが加速すると予想されます。
日本においては、法的規制や社会的認識の壁を乗り越える必要がありますが、基礎研究の促進、国際共同研究への参加、法規制の見直し検討などから始めることが現実的でしょう。厚生労働省の「依存症対策推進基本計画」でも科学的根拠に基づいた対策の推進が掲げられており、エビデンスが蓄積されれば政策面での検討も進む可能性があります。
サイケデリック療法は、従来の治療法では効果が不十分だった患者に新たな希望をもたらす可能性を秘めています。個別化医療の観点から、どのような患者に効果があるかの研究も進められています。適切な規制のもとで研究を進め、安全性と有効性を確立することで、日本の依存症治療の選択肢を広げることができるでしょう。
Bogenschutz, M. P., Forcehimes, A. A., Pommy, J. A., Wilcox, C. E., Barbosa, P. C. R., & Strassman, R. J. (2015). Psilocybin-assisted treatment for alcohol dependence: A proof-of-concept study. Journal of Psychopharmacology, 29(3), 289-299.
Bogenschutz, M. P., Ross, S., Bhatt, S., Baron, T., Forcehimes, A. A., Laska, E., et al. (2022). Percentage of heavy drinking days following psilocybin-assisted psychotherapy vs placebo in the treatment of adult patients with alcohol use disorder: A randomized clinical trial. JAMA Psychiatry, 79(10), 953-962.
Johnson, M. W., Garcia-Romeu, A., Cosimano, M. P., & Griffiths, R. R. (2014). Pilot study of the 5-HT2AR agonist psilocybin in the treatment of tobacco addiction. Journal of Psychopharmacology, 28(11), 983-992.
Johnson, M. W., Garcia-Romeu, A., & Griffiths, R. R. (2017). Long-term follow-up of psilocybin-facilitated smoking cessation. American Journal of Drug and Alcohol Abuse, 43(1), 55-60.
van der Meer, P. B., Fuentes, J. J., Kaptein, A. A., Schoones, J. W., de Waal, M. M., Goudriaan, A. E., et al. (2023). Therapeutic effect of psilocybin in addiction: A systematic review. Frontiers in Psychiatry, 14, 1134454.
Zafar, R., Siegel, M., Harding, R., Barba, T., Agnorelli, C., Suseelan, S., et al. (2023). Psychedelic therapy in the treatment of addiction: The past, present and future. Frontiers in Psychiatry, 14, 1183740.
本記事は情報提供のみを目的としており、医療アドバイスではありません。
精神的・身体的な問題を抱えている方は、必ず医療専門家にご相談ください。
また、日本国内でのサイケデリック物質の所持・使用は法律で禁止されています。





